CIC - Centre d’Investigation Clinique
Résumé, définition
Structures mixtes INSERM/DGOS réparties sur l’ensemble du territoire qui sont dédiées à l’investigation clinique et translationnelle allant des phases précliniques aupost-market. Les instituts ont pour fonction la promotion, l’aide méthodologique, la gestion de données, les bio-statistiques et l’aide à l’acquisition des données dans les projets de recherches cliniques.
Leur typologie intègre différents modules plurithématiques, pharmacologique, épidémiologique, biothérapie et innovation technologique. Leur rôle est d’offrir un espace d’accompagnement à la recherche appliquée.
Les modules IT (Innovation Technologique) ont particulièrement un rôle dans la proposition d’innovations technologiques et dans le développement de collaborations industrielles et institutionnelles pour faciliter l’émergence de nouveaux DM. L’originalité de leur mission est d’accompagner le chercheur/utilisateur depuis l’élaboration du concept jusqu’à la mise sur le marché. Ceci dans un environnement intégrant les aspects d’assurance qualité et de réglementation.
Ils sont en mesure de collaborer avec les Living Labs lorsque les problématiques d’usage le justifient et, le cas échéant, de prendre en compte les résultats de travaux de co-conception ou d’évaluation d’usage réalisés en amont par ces structures.
Chaque projet soumis à un CIC doit prévoir son financement : investigation clinique, accompagnement réglementaire et/ou méthodologique, gestion des données et personnels dédiés. Le CIC prenant à sa charge le coût des personnels permanents et de l’environnement.
Le parcours
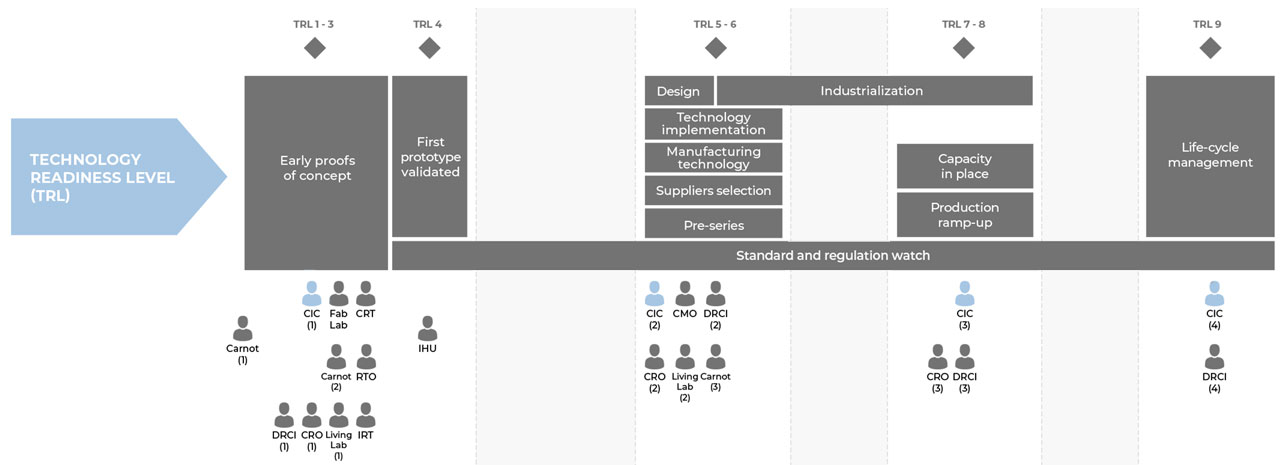
L’implantation hospitalière des CIC procure l’appui nécessaire des personnes utilisatrices des innovations et leur implication dans des expérimentations précoces puis tout au long du développement.
Les CIC ont ainsi mis en place des lieux d’expérimentation (« simulateurs d’expérimentation ») et des lieux autorisés pour des premiers tests chez l’homme dans un environnement hautement sécurisé. Dans ces lieux, tous les acteurs peuvent se confronter au terrain et bénéficier des expertises médicales et de patients et ainsi identifier rapidement les solutions pertinentes ou au contraire impraticables.
(1) TRL 1-4
Le chercheur/utilisateur souhaitant développer une idée peut prendre contact avec les CIC (IT) avant de s’engager dans le design du projet. Il peut avoir préalablement affiné cette idée dans un Living Lab ou être invité à le faire selon le poids de la problématique d’usage et d’appropriation.
Expertise sur la pertinence de l’idée et du besoin sociétal, évaluation des besoins organisationnels et orientation vers réseaux de compétence (par exemple réseau CICIT, Tech4health…).
Aide au développement technologique y compris sur les phases précliniques.
(2) TRL 5
Chercheur/utilisateur souhaitant débuter les premières validations cliniques (par exemple first-in-man d’un prototype de DM).
(3) et (4) TRL 7-9
Aide à la réalisation des essais cliniques une fois le dispositif manufacturé (aide au marquage CE, à l’accès au marché et/ou au remboursement). Les Living Labs peuvent être mobilisés conjointement si les problématiques d’usage le justifient.
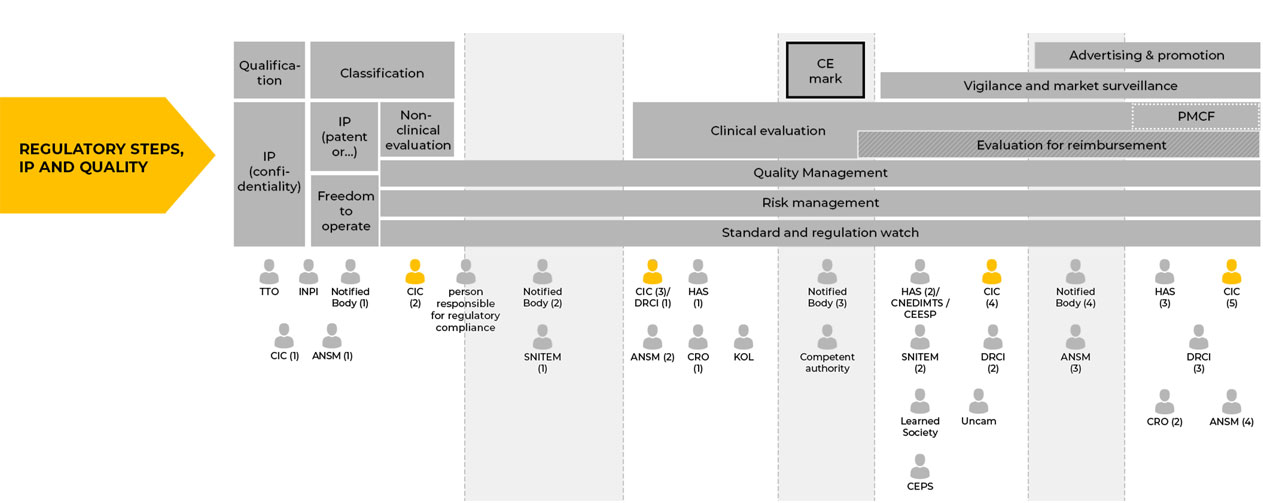
(1)
lP : mise en lien entre chercheur/utilisateur avec les organismes de valorisation (ex : accord de confidentialité, rédaction de déclaration d’invention aide au dépôt de brevet).
(2)
Aide à la soumission réglementaire si besoin.
(3) avec DRCI
Aide à la valorisation scientifique (Ex : communication des résultats de l’étude)/remplissage clinical Trial /Publications.
(4)
Accompagnement pour le respect et l’application des obligations légales de l’investigateur et/ou du promoteur (ex : monitoring de l’étude, gestion des événements indésirables).
(5)
La localisation des CIC dans les centres de soins favorise les travaux autour des données de santé, leur sécurité, leur exploitation. On parle alors de surveillance, d’études de suivi post-commercialisation, à travers la mise en œuvre et la tenue de registres, le suivi de cohortes. Ces travaux génèrent une activité nouvelle de « matério-épidémiologie ».
Le nombre croissant d’objets connectés engendre un volume de données conséquent et nécessite l’organisation de leur gestion et la mise en place de centres agréés (à l’instar des hébergeurs agréés par l’ASIP santé : agence française de la santé numérique).
Ressources Internet
https://www.inserm.fr/recherche-inserm/recherche-clinique/centres-investigation-clinique-cic
CIC-IT de Besançon : https://www.fc-sante.fr/cic-besancon/centre_investigation_clinique_recherche_page/accueil.php
CIC-IT de Bordeaux : http://www.cic-it-bordeaux.fr/
CIC-IT de Garches (Paris) : http://www.cic-it.fr/cic-it-paris.php
CIC-IT de Grenoble : http://www.chu-grenoble.fr/content/centre-dinvestigation-clinique-innovation-technologique-cic-it
CIC-IT de Lille : http://www.cic-it-lille.com/
CIC-IT de Nancy : http://www.cic-it-nancy.fr/fr/
CIC-IT de Rennes : http://cic.chu-rennes.net/?q=cic-it/structure
CIC-IT de Tours : http://cic-it-tours.fr/

