HAS - Haute Autorité de Santé
Résumé, définition
La Haute Autorité de Santé est une autorité publique indépendante qui « évalue d’un point de vue médical et économique les produits, actes, prestations et technologies de santé en vue de leur remboursement ». Elle a un rôle d’aide à la décision des pouvoirs publics pour le remboursement des produits de santé, des actes et prestations.
Elle se compose de plusieurs commissions dont :
– La CNEDiMTS : Commission nationale d’évaluation des dispositifs médicaux et technologies de santé ;
– La CEESP : Commission d’évaluation économique et de santé publique.
Le parcours
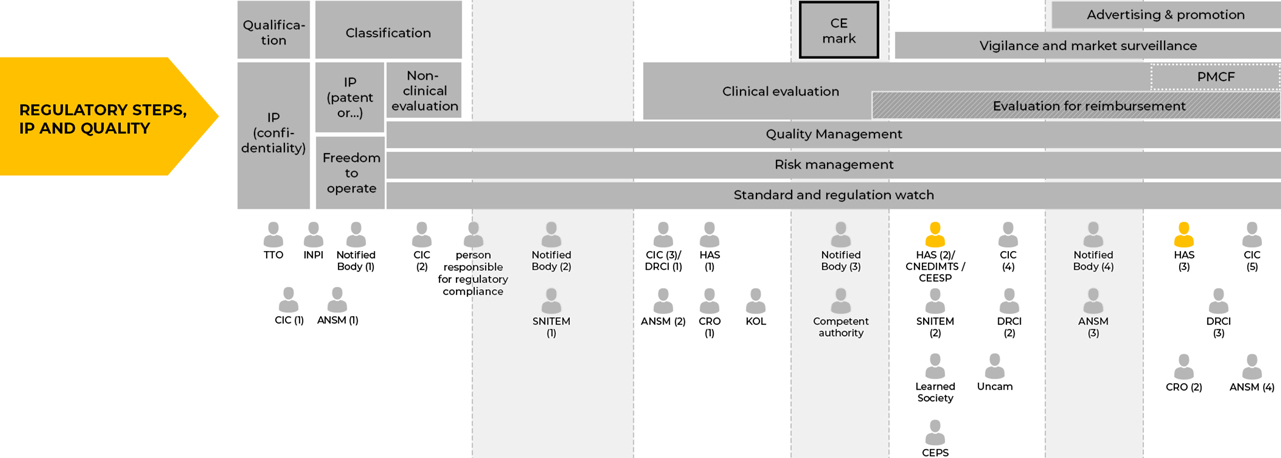
(1) Clinical evaluation
Au cours du développement clinique du DM : une entreprise peut solliciter une « rencontre précoce » auprès des services de la HAS pour échanger sur la pertinence d’un protocole d’étude clinique ou médico-économique[1] en vue du remboursement.
[1] Dans le cas où une étude médico-économique devrait être soumise à la CEESP (Commission d’évaluation économique et de santé publique)
(2) Evaluation for reimbursement
En vue du dépôt d’un dossier de demande de remboursement : une entreprise qui souhaite déposer une demande d’inscription sur la liste des produits et prestations (LPP) peut solliciter, avant le dépôt de son dossier, un « rendez-vous pré-dépôt » auprès des services de la HAS.
La CNEDiMTS évalue les dossiers de demande de remboursement des DM et donne son avis sur leur éligibilité au remboursement sur la base des données fournies par l’entreprise. Elle évalue également les actes professionnels nécessaires à l’utilisation des DM (ex : acte de pose d’un DM implantable).
La CEESP évalue l’efficience des DM innovants et susceptible d’avoir un impact significatif sur les dépenses de santé.
(3)
Lorsqu’elle rend son avis sur l’inscription d’un DM au remboursement, la CNEDiMTS précise, le cas échéant, si des données complémentaires seront nécessaires lors du renouvellement de l’inscription. Dans ce cas, l’entreprise doit prévoir la mise en place d’une étude post-inscription.

(1) Public Research Funding
La HAS a un rôle important dans le cadre du forfait innovation :
– Elle rencontre les entreprises qui ont un projet de dépôt de demande de forfait innovation concernant la pertinence de la demande (données critiques manquantes) et la méthodologie (objectifs, critères de jugement, plan expérimental de l’étude…).
– Via un jury dédié, une fois le dossier déposé par l’entreprise, elle évalue le caractère innovant de la technologie et la pertinence du protocole de l’étude. Elle transmet son avis au ministère en charge de la santé.
Ressources Internet
site de la HAS : http://www.has-sante.fr
http://social-sante.gouv.fr/ministere/acteurs/partenaires/article/has-haute-autorite-de-sante
CNEDiMTS :https://www.has-sante.fr/portail/jcms/c_929613/fr/que-fait-la-cnedimts
Documents et guides de la HAS :
- Parcours du dispositif médical en France, guide pratique (document pdf, novembre 2017) :
- Document exposant les principes d’évaluation de la CNEDiMTS relatifs aux dispositifs médicaux à usage individuel en vue de leur accès au remboursement (document pdf, m ;a.j ; mai 2019) :
- Guide spécifique pour le remboursement d’un DM connecté
- Cette page traite des rencontres précoces avec la HAS pour échanger sur un projet d’étude clinique en vue d’un dossier de remboursement
- Il existe également un guide avec les modalités et le déroulement de la soumission du dossier de remboursement.
- Des informations sont également disponibles sur les rendez-vous pré-dépôt sur des questions concrètes au moment où l’industriel préparer son dossier de remboursement :
- sur le forfait innovation : prise en charge dérogatoire et transitoire de technologies de santé innovantes lorsqu’elles sont en phase précoce de développement clinique

