user - User / prescriber / patient / customer
Résumé, définition
Pour les dispositifs médicaux, de nombreux usagers sont possibles :
- l’utilisateur d’un dispositif médical peut être le patient ou le professionnel de santé (médecin, chirurgien, infirmier…)
- le prescripteur : médecin (il n’est pas forcement l’utilisateur)
- l’acheteur peut être le patient, le centre de soins, le médecin
- le patient est le client bénéficiaire final.
Toutefois, pour certains DM, les termes peuvent être ambigus : par exemple dans le cas d’un DM implantable, appelé à rester dans le corps du patient, on peut comprendre utilisateur à la fois comme le chirurgien qui va poser le dispositif médical et le patient qui va le garder.
De la même manière, il faut faire la différence entre le prescripteur et l’acheteur. Ces acteurs sont essentiels pour la réalisation du business plan : l’utilisateur et le prescripteur devront convaincre ses acheteurs d’acheter le DM !
Le parcours
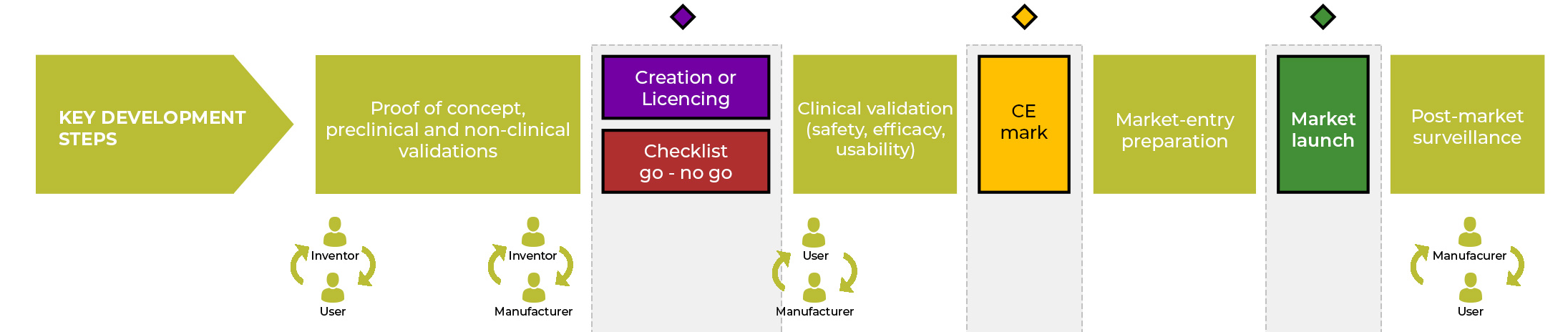
Renvoyer vers la fiche « interactions »
(1)
Pour développer, comprendre le besoin et identifier les utilisations du DM dans le parcours de soin.
Des contacts avec les cliniciens doivent avoir lieu très tôt pour limiter le “techno-push” (Ce n’est pas parce qu’un DM peut technologiquement exister qu’il a un réel intérêt ou qu’il pourra être mis sur le marché visé).
Il faut aussi prendre en considération l’articulation des différents intervenants (médecin, infirmier, prestataire…). Les DM sont de plus en plus connectés entre eux et entre utilisateurs (patients/soignants). L’organisation des soins et la définition du rôle de chacun est cruciale au moment de la diffusion du produit. C’est un point à anticiper.
Dès les premières étapes de la conception d’un DM, il faut prendre en considération l’aptitude à l’utilisation. La norme 62366 vise à prévenir les dangers dus aux erreurs d’utilisation d’un dispositif médical. Sa mise en application doit permettre une utilisation intuitive des dispositifs, ce qui est critique à l’heure où le patient devient de plus en plus son propre soignant (par exemple pour dispositifs utilisés au domicile).
Par exemple : un environnement technique particulier doit-il être mis en place? pour une première phase de diffusion, un encadrement des opérateurs et de l’environnement technique peut permettre de d’optimiser les résultats si le DM nécessite un entraînement particulier.
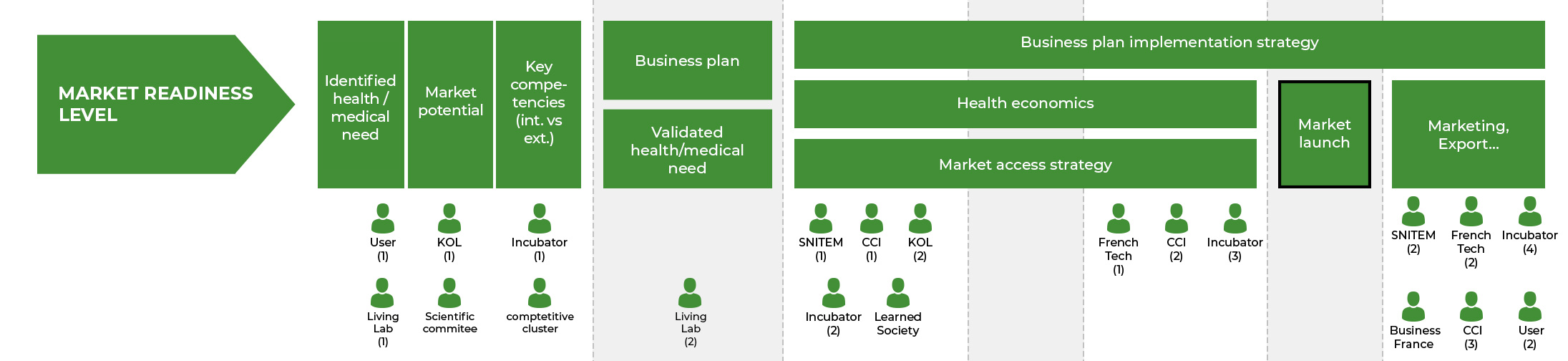
(2)
Convaincre d’acheter : en lien avec la publicité, qui est réglementée (plus de renseignements sur le site de l’ANSM).
Post-market surveillance : déclaration d’effets indésirables et matériovigilance.
Comme stipulé dans le règlement : « Il y a lieu d’encourager les professionnels de la santé, les utilisateurs et les patients et de leur permettre de notifier les incidents graves supposés au niveau national selon des modalités harmonisées»
https://eur-lex.europa.eu/legal-content/EN/TXT/?qid=1516896388241&uri=CELEX:32017R0745
/!\ Les établissements publics ou certaines centrales d’achat sont soumis au code des marchés publics.
Identifier selon le type de produit, les pharmaciens monopole sur DM stérile et/ou implantable et les biomédicaux sur les « machines ». Une machine nécessitant des consommables stériles devra être vu par les 2 interlocuteurs.
/!\ Quel est le circuit de distribution (Ville ?Hôpital ?Particulier ?) car les règles de distributions diffèrent.

